domingo, 13 de noviembre de 2016
Test ácidos nucleicos
Este ha sido el resultado del test en el que he respondido unas preguntas sobre los ácidos nucleicos. Cabe destacar que me ha parecido una forma más amena de comprobar nuestros conocimientos.
Esquema tema 6: "Ácidos nucleicos"
En estas imágenes podéis observar el esquema del sexto tema de biología de 2ºBAT: "Ácidos nucleicos". He dividido el esquema en composición, ADN y ARN.
Los ácidos nucleicos están compuestos por cadenas de nucleótidos y cada nucleótido está formado por un nucleósido (pentosa y base nitrogenada) y un ácido fosfórico. También se muestran los enlaces que unen los distintos compuestos.
Existen dos tipos de ácidos nucleicos: ADN y ARN. El ADN contiene desoxirribosa como pentosa y como bases nitrogenadas encontramos la adenina, guanina, citosina y timina. En cambio, en el ARN la pentosa es una ribosa y las bases nitrogenadas son la adenina, guanina, citosina y uracilo. Además, en el esquema se puede ver la clasificación del ADN (según el tipo de célula, número de cadena y forma, la molécula que participa en el empaquetamiento o el ADN supernumerario) y su estructura (primaria, secundaria y terciaria). De igual forma, en el ARN encontramos su estructura (bicatenaria o monocatenaria) y los tipos de ARN (ARNm, ARNt, ARNr, ARNn, ARNpn y ARNi) y sus funciones.



Los ácidos nucleicos están compuestos por cadenas de nucleótidos y cada nucleótido está formado por un nucleósido (pentosa y base nitrogenada) y un ácido fosfórico. También se muestran los enlaces que unen los distintos compuestos.
Existen dos tipos de ácidos nucleicos: ADN y ARN. El ADN contiene desoxirribosa como pentosa y como bases nitrogenadas encontramos la adenina, guanina, citosina y timina. En cambio, en el ARN la pentosa es una ribosa y las bases nitrogenadas son la adenina, guanina, citosina y uracilo. Además, en el esquema se puede ver la clasificación del ADN (según el tipo de célula, número de cadena y forma, la molécula que participa en el empaquetamiento o el ADN supernumerario) y su estructura (primaria, secundaria y terciaria). De igual forma, en el ARN encontramos su estructura (bicatenaria o monocatenaria) y los tipos de ARN (ARNm, ARNt, ARNr, ARNn, ARNpn y ARNi) y sus funciones.



sábado, 5 de noviembre de 2016
Esquema tema 5: "Las proteínas"
En la siguiente imagen muestro el esquema del quinto tema de
biología de 2ºBAT: "Las proteínas". Como podemos observar, he
dividido el esquema en dos grandes bloques: la estructura y la clasificación.
Dentro de la estructura encontramos la estructura primaria, secundaria, terciaria y cuaternaria. En la estructura primaria hallamos los aminoácidos y sus propiedades físicas y químicas, su clasificación, su estructura y el enlace peptídico. En la estructura secundaria vemos los distintos tipos que existen: estructura en α-hélice, estructura de la hélice del colágeno y conformación-β. En la estructura terciaria podemos observar los enlaces, dominios estructurales y las dos clases de proteínas que la contienen (filamentosas y globulares). En la estructura cuaternaria también encontramos los tipos de enlaces que la forman.
Por otra parte, he clasificado las proteínas en holoproteínas y heteroproteínas. Dentro de las primeras podemos ver las filamentosas y las globulares, y dentro de las heteroproteínas podemos encontrar las cromoproteínas, glucoproteínas, lipoproteínas, fosfoproteínas y nucleoproteínas.
Proteínas
1. Con respecto a las proteínas:
a) Enumerar los
cuatro niveles de estructura de las proteínas.
Podemos diferenciar cuatro
niveles de estructura de las proteínas:
 |
| Fuente: wikipedia |
b) Indicar qué tipos de enlaces
intervienen en la estabilización de cada uno de estos niveles estructurales.
En la estructura primaria
intervienen enlaces peptídicos que unen
los distintos aminoácidos y enlaces
covalentes que unen el grupo carboxilo, el grupo amino, el hidrógeno y el
radical con el carbono alfa.
En la estructura secundaria se
encuentran enlaces puentes de hidrógeno.
En la estructura terciaria se
diferencian enlaces débiles y enlaces fuertes. Los enlaces débiles son enlaces de hidrógenos, interacciones iónicas, fuerzas de Van der Walls e interacciones hidrofóbicas. Los enlaces
fuertes son los enlaces disulfuro.
En la estructura cuaternaria, las
cadenas polipeptídicas se unen a través de enlaces
débiles (no covalentes) y si presenta cisteína, enlaces disulfuro.
c) Especificar la estructura que
caracteriza a las α-queratinas.
Las
α-queratinas están formadas por una estructura en α-hélice. Esta
estructura es un tipo de estructura secundaria.
d) Describir dos propiedades generales
de las proteínas.
Solubilidad:
Esta
propiedad no se da en todo tipo de proteínas, solo en las globulares. Los
radicales polares de los aminoácidos de estas proteínas les aportan solubilidad
ya que se unen a las moléculas de agua mediante puentes de hidrógeno. De esta
manera cada radical queda recubierto de agua impidiendo que se pueda unir a
otras moléculas proteicas y provocando su precipitación.
Si
el pH varía, modifica el grado de ionización de los radicales polares
influyendo así en la solubilidad.
Especificidad:
Las
proteínas que interactúan con otras moléculas tienen una estructura específica
y unos aminoácidos concretos que les permiten diferenciar unas moléculas de
otras.
Por
ejemplo, las proteínas enzimáticas poseen un conjunto de aminoácidos (centro
activo) que le permite reconocer un sustrato específico.
Además
existen proteínas homólogas que tienen la misma función y una estructura
parecida pero no idéntica ya que se diferencia en algunos aminoácidos que, al
sustituirlos, no alteran su función. Esto provoca problemas en los trasplantes
de órganos
e) Describir dos funciones de las proteínas. Indica ejemplo.
Enzimática: las enzimas son proteínas que actúan como
biocatalizadores aumentando la velocidad de las reacciones químicas y
disminuyendo la energía de activación. Por ejemplo, la maltasa y la lipasa.
Homeostática: las proteínas se encargan de mantener constantes los
valores del medio interno (salinidad, acidez, concentración glucosa…). Por
ejemplo, la trombina y fibrinógeno que intervienen en la coagulación sanguínea
evitando hemorragias.
f) Defina el proceso de desnaturalización. ¿Qué tipo de enlaces no se ven
afectados?
La desnaturalización de una proteína
es la pérdida de la estructura cuaternaria, terciaria y, a veces, la secundaria.
Se debe a la rotura de los enlaces que la componen a excepción de los enlaces
peptídicos. La rotura se produce por variaciones de pH, temperatura, concentración
de sales o por agitación molecular. Como consecuencia de la pérdida de la
estructura, también dejan de realizar las funciones.
Cuando una proteína se
desnaturaliza, las moléculas de agua no recubren totalmente la proteína y estas
tienden a unirse con otras moléculas proteicas, dando lugar a una conformación
filamentosa y a su precipitación.
Además como este proceso no
afecta a los enlaces peptídicos, la proteína se puede renaturalizar si se
vuelve a las condiciones normales.
 |
| Fuente. wikipedia |
g) ¿Qué significa que un aminoácido es anfótero?
Los aminoácidos tienen carácter anfótero si se
encuentran en disolución acuosa. Esto significa que pueden actuar como bases o
como ácidos originando una forma iónica dipolar gracias a que el grupo carboxilo libera protones y el grupo amino los capta.
El pH en el que se encuentra esta forma dipolar neutra se llama punto isoeléctrico. Cuando el aminoácido se encuentra en este punto, si se acidifica
el medio el grupo carboxilo ionizado actúa como base y capta protones .
En cambio si se basifica el medio, y el grupo amino ionizado se comporta como ácido y libera protones.
Gracias a esto, se dice que
tienen una gran capacidad amortiguadora.
sábado, 29 de octubre de 2016
Lípidos
A continuación, responderé a unas preguntas sobre los lípidos:
b) ¿En qué estructura celular se localizan mayoritariamente los fosfolípidos?
c) Explique qué significa que los fosfolípidos son compuestos anfipáticos y su implicación en la organización de dicha estructura.
1. Con respecto a los fosfolípidos:
a) Explique su composición química, haciendo referencia al tipo de enlaces que unen a sus componentes.
Dentro de los fosfolípidos encontramos:
- Fosfoglicéridos: compuestos por dos ácidos grasos, una glicerina, un ácido fosfórico y un aminoalcohol como la serina.
- Fosfoesfingolípidos: compuestos por un ácido graso, una esfingosina, un ácido fosfórico y un aminoalcohol como la colina.
En todos los fosfolípidos, los elementos que los constituyen están unidos a través de un enlace de tipo éster.
a) Explique su composición química, haciendo referencia al tipo de enlaces que unen a sus componentes.
Dentro de los fosfolípidos encontramos:
- Fosfoglicéridos: compuestos por dos ácidos grasos, una glicerina, un ácido fosfórico y un aminoalcohol como la serina.
- Fosfoesfingolípidos: compuestos por un ácido graso, una esfingosina, un ácido fosfórico y un aminoalcohol como la colina.
En todos los fosfolípidos, los elementos que los constituyen están unidos a través de un enlace de tipo éster.
b) ¿En qué estructura celular se localizan mayoritariamente los fosfolípidos?
Los fosfolípidos se localizan mayoritariamente en la membrana plasmática, por eso también se llaman lípidos de membrana.
Significa que poseen una parte hidrófila que se corresponde al grupo fosfato y al aminoalcohol y una parte hidrófila que son los ácidos grasos y, dependiendo del tipo de fosfolípido, la glicerina o la esfingosina.
Gracias a esta característica, pueden formar una o dos capas en las la parte hidrófoba se dispone hacia el interior y la hidrófila que lo hace hacia el exterior.
Gracias a esta característica, pueden formar una o dos capas en las la parte hidrófoba se dispone hacia el interior y la hidrófila que lo hace hacia el exterior.
2. Los lípidos son moléculas orgánicas presentes en todos los seres vivos con una gran heterogeneidad de funciones.
a) Indique la composición química de un triacilglicérido de origen vegetal.
La trioleína es un triacilglicérido que presenta ácidos grasos insaturados y forma el aceite de oliva.
b) La obtención del jabón se basa en una reacción en la que intervienen algunos lípidos; explique esta reacción e indique cómo se denomina.
Esta reacción se denomina de saponificación. Se produce cuando un ácido graso reacciona con una base fuerte como el NaOH o el KOH y da lugar a la sal de un ácido que pasa a llamarse jabón.
c) Justifique si el aceite de oliva empleado en la cocina podría utilizarse para la obtención de jabón.
El aceite de oliva empleado en la cocina sí podría utilizarse en la obtención de jabón porque el aceite es un ácido graso con un grupo carboxilo y si se hace reaccionar con una base como el NaOH, se obtiene el grupo -COONa que ioniza fuertemente. Esto hace que el jabón obtenido sea buen emulsionante y dispersante, es decir, que dispersa los lípidos en el agua.a) Indique la composición química de un triacilglicérido de origen vegetal.
La trioleína es un triacilglicérido que presenta ácidos grasos insaturados y forma el aceite de oliva.
b) La obtención del jabón se basa en una reacción en la que intervienen algunos lípidos; explique esta reacción e indique cómo se denomina.
Esta reacción se denomina de saponificación. Se produce cuando un ácido graso reacciona con una base fuerte como el NaOH o el KOH y da lugar a la sal de un ácido que pasa a llamarse jabón.
 |
| Fuente: libro |
c) Justifique si el aceite de oliva empleado en la cocina podría utilizarse para la obtención de jabón.
3. Dada la siguiente estructura indique:
- ¿Qué tipo de molécula se muestra?
b) Indique las principales propiedades físicas y químicas de este grupo de moléculas.
En cuanto a las propiedades físicas y químicas, los acilglicéridos son insolubles en el agua, saponificables ( reaccionan con bases para dar lugar a jabones) y apolares ya que no poseen ningún radical hidroxilo (-OH) libre. Además son buenos aislantes térmicos y tienen función de reserva energética.
c) En los organismos vivos animales y vegetales ¿dónde encontraría este tipo de moléculas?
Este tipo de moléculas las podemos encontrar en las vacuolas de las células vegetales y en los adipocitos de los animales.
Este tipo de moléculas las podemos encontrar en las vacuolas de las células vegetales y en los adipocitos de los animales.
sábado, 22 de octubre de 2016
Esquema tema 4: "Los lípidos"
Aquí os muestro el esquema que he hecho del tercer tema de biología de 2ºBAT: "Los lípidos". Como podemos observar, he clasificado los lípidos en ácidos grasos, saponificables e insaponificables. En los ácidos grasos encontramos los saturados, los insaturados y sus propiedades físicas, químicas y biológicas. Por otro lado, dentro de los saponificables están los simples (acilglicéridos y céridos) y los complejos (fosfoglicéridos, fosfoesfingolípidos y glucoesfingolípidos). Por último, los insaponificables los clasificamos en isoprenoides, esteroides y prostaglandinas.
Práctica reconocimiento de glúcidos
El otro día realizamos una práctica en el laboratorio sobre el reconocimiento de glúcidos. Una vez terminada podemos responder a las siguientes preguntas:
1. ¿Qué azúcares son reductores? ¿Por qué?
Los azúcares reductores son la glucosa, la lactosa, la maltosa, el zumo de uva, el azúcar de caña, la leche entera, la cerveza y la sacarosa solamente cuando se mezcla con el ácido clorhídrico. Estos azúcares son reductores porque poseen un enlace monocarbonílixo, es decir, el grupo hidroxilo del carbono anomérico del primer monosacárido se une con el segundo monosacárido por un grupo alcohol de un carbono no anomérico. De esta forma el carbono anomérico del segundo monosacárido queda libre y reduce el Reactivo de Fehling.
2. ¿Qué ocurre en el tubo 2? y ¿en el 10?
El tubo 2 no cambia de color porque la sacarosa no reduce el Reactivo de Fehling y en el tubo 10 se mezcla la sacarosa y el ácido clorhídrico lo que hace que sí cambie de color.
3. ¿Qué función tiene el ácido clorhídrico?
El ácido clorhídrico hace que la sacarosa se descomponga en los dos monosacáridos que la forman: glucosa y fructosa. Estos sí son reductores y por eso sí cambia de color.
4. ¿Dónde produce nuestro cuerpo ácido clorhídrico?
Nuestro cuerpo produce ácido clorhídrico en el estómago.
5.
Los diabéticos eliminan glucosa por la orina ¿Cómo se puede diagnosticar la
enfermedad?
Esta enfermedad se diagnostica haciendo la prueba del Reactivo de Fehling a la orina y si sale positivo, es decir, si cambia de color significa que sí tiene glucosa.
domingo, 16 de octubre de 2016
Esquema tema 3: "Los glúcidos"
En la siguiente imagen podréis ver el esquema del tercer tema de biología de segundo de bachiller: "Los glúcidos". En él se diferencian los dos tipos de glúcidos: holósidos y ósidos. En los holósidos encontramos las características biológicas, físicas y químicas, y la isomería. Por otro lado, los ósidos se dividen en heterósidos y holósidos, y dentro de ellos observamos sus distintos tipos. Por último, vemos los dos tipos de proyecciones que existen: Fisher y Haworth.
Glúcidos
A continuación, responderé a unas preguntas sobre los glúcidos:
1) La D-glucosa es una aldohexosa.
1) La D-glucosa es una aldohexosa.
Explica:
a) ¿Qué significa ese término?
Ese término significa que es un monosacárido formado por una molécula de seis carbonos. Además contiene un grupo aldehído (-CHO) en el primer carbono y grupos hidroxilo (-OH) en el resto de carbonos.
b) ¿Qué importancia biológica tiene la glucosa?
A partir de la glucosa los seres vivos obtenemos energía mediante la respiración celular que se produce en las mitocondrias de las células:
C2H12O6 + 6O2 => 6CO2 + 6H2O+ 36ATP
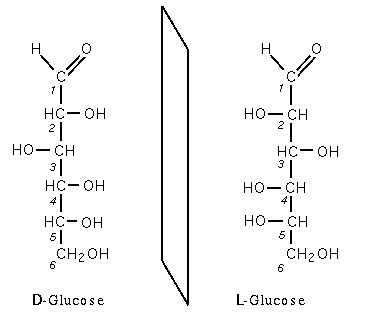
c) ¿Qué diferencia existe entre la D-glucosa y la L-glucosa, y entre la α y la β D- glucopiranosa?
La D-glucosa y la L-glucosa se tratan de enantiómeros, es decir, son imágenes especulares entre sí. En la D-glucosa el -OH del carbono asimétrico más alejado del grupo carbonilo está a la derecha y en la L-glucosa se sitúa en la izquierda.
 |
| Fuente: wikipedia |
Por otro lado, en la ciclación de una molécula aparece un nuevo carbono asimétrico al que se le denomina carbono asimétrico. En la α-D-glucopiranosa el grupo hidroxilo del cabrono anomérico queda al contrario que el grupo CH2OH y en la β-D-glucopiranosa queda en el mismo lado que dicho grupo.
 |
| Fuente: wikipedia |
2) Dentro de un grupo de biomoléculas orgánicas se puede establecer la clasificación de:
monosacáridos, oligosacáridos y polisacáridos.
Homopolisacáridos y heteropolisacáridos
Función energética (reserva) y función estructural.
a) cita un ejemplo diferente para cada uno de los tipos diferenciados en la clasificación 1, 2 y 3 (total 7 moléculas).
- Monosacárido: glucosa
- Oligosacárido: maltosa
- Polisacárido: almidón
- Homopolisacárido: glucógeno
- Heteropolisacárido: pectina
- Función energética: glucógeno
- Estructural: celulosa
- Oligosacárido: maltosa
- Polisacárido: almidón
- Homopolisacárido: glucógeno
- Heteropolisacárido: pectina
- Función energética: glucógeno
- Estructural: celulosa
b) ¿En base a qué criterio se establece la clasificación número 2 ?
Los polisacáridos están compuestos por más de diez monosacáridos y se diferencian en dos grupos. Los homopolisacáridos están formados por el mismo monosacárido y los heteropolisacáridos se constituyen de diferentes monosacáridos.
3) En relación a los glúcidos:
a) Indica cuál de los siguientes compuestos son monosacáridos, disacáridos o polisacáridos: sacarosa, fructosa, almidón, lactosa, celulosa y glucógeno.
La fructosa es un monosacárido.
La sacarosa y la lactosa son disacáridos.
El almidón, la celulosa y el glucógeno son polisacáridos.
b) Indica en qué tipo de organismos se encuentran los polisacáridos indicados en el
apartado anterior.
El glucógeno se encuentra en los animales y el almidón y la celulosa se encuentran en los vegetales.
c) Indica cuál es la función principal de los polisacáridos indicados en el apartado a).
El glucógeno y el almidón tienen función de reserva energética y la celulosa tiene función estructural.
d) Cita un monosacárido que conozcas y que no se encuentre en la relación incluida en el apartado a).
La galactosa.
4) Realiza todos los pasos de la ciclación de una D-galactosa hasta llegar a una α-D- galactopiranosa.
viernes, 7 de octubre de 2016
Esquema tema 2: "Los bioelementos, el agua y las sales minerales"
Este es el esquema que he realizado sobre el segundo tema del libro de biología de 2ºBAT: "Los bioelementos, el agua y las sales minerales". Como podemos observar, he partido de la palabra "bioelementos" diferenciándolos entre primarios y secundarios y, posteriormente, mostrando los tipos de biomoléculas simples o compuestas y orgánicas o inorgánicas. Por último, me he centrado en explicar la estructura y propiedades del agua además de los tipos de sales minerales y sus propiedades.
Ósmosis
En esta imagen os muestro un esquema dibujado que hemos realizado en clase sobre la ósmosis. En él observamos el comportamiento de una célula vegetal y una animal en los distintos tipos de medios en los que se puede encontrar la célula:
-Isotónico: la concentración de sales minerales es igual en el interior y exterior de la célula, por lo que no se deforma.
-Hipotónico: la concentración de sales minerales es más baja en el exterior. Para igualar dicha concentración, el agua entra a la célula y esta se hincha. La célula animal puede llegar a explotar (hemolisis), pero la vegetal no ya que está protegida por la pared celular (turgencia).

-Isotónico: la concentración de sales minerales es igual en el interior y exterior de la célula, por lo que no se deforma.
-Hipotónico: la concentración de sales minerales es más baja en el exterior. Para igualar dicha concentración, el agua entra a la célula y esta se hincha. La célula animal puede llegar a explotar (hemolisis), pero la vegetal no ya que está protegida por la pared celular (turgencia).
-Hipertónico: la concentración de sales minerales es más alta fuera de la célula. La concentración se iguala cuando el agua sale de la célula y se arruga. La célula animal puede llegar a morir (crenación), pero la vegetal no debido a los puntos de unión entre la membrana y la pared celular (plasmolisis).

domingo, 25 de septiembre de 2016
Todos somos agua
 |
| Fuente. Wikipedia |
En cuanto a sus propiedades y funciones, podemos destacar las siguientes:
- Elevada fuerza de cohesión: debido a los puentes de hidrógeno el agua es casi incompresible. Esto permite que tenga función estructural (turgencia y formación de esqueletos hidrostáticos) y que sea un buen amortiguador mecánico (líquido sinovial).
- Elevada fuerza de adhesión: las moléculas de agua se adhieren las paredes de los conductos ascendiendo a través de ellos en contra de la gravedad (capilaridad). Esta propiedad posibilita que el agua sea un buen transportador (sangre y savia bruta).
- Elevada tensión superficial: la superficie del agua opone gran resistencia a romperse. Gracias a esto, es posible la vida de organismos asociados a su superficie (zapatero) y la formación de líquidos que evitan el roce de los huesos (líquido sinovial).
- Elevado calor específico: es la cantidad de calor necesaria para elevar la temperatura de una unidad de masa de sustancia en un grado. Los puentes de hidrógeno son muy importantes en esta propiedad y permiten que el agua sea un buen termorregulador.
- Elevado calor de vaporización: se necesita mucha energía para romper los puentes de hidrógeno y pasar de estado líquido a gaseoso. El agua que se evapora en la superficie de un ser vivo absorbe el calor del organismo, por eso es un buen refrigerante.
- Elevada densidad en estado líquido: el agua es más densa en estado líquido que en estado sólido, lo que hace que haya vida en mares, ríos y lagos donde su superficie esté congelada.
- Elevada constante dieléctrica: las moléculas de agua rodean los iones y las moléculas de otras sustancias (solvatación) lo que implica que sea un buen disolvente y un buen reactivo.
- Bajo grado de ionización: pocas moléculas de agua se encuentran ionizadas por lo que la concentración de protones e hidroxilos es baja. Si se le añade un ácido o una base, los niveles varían bruscamente.
Para finalizar, os dejo una infografía que he realizado junto a mi grupo (Ana Bas, Andrés Felipe y Reme García) sobre este tema:
lunes, 19 de septiembre de 2016
Reflexión
Comenzaré esta reflexión tratando el significado de esta asignatura para mi. Personalmente, opino que la biología es una ciencia muy interesante y está inmersa en la sociedad actual, desde el campo de la medicina hasta el de la tecnología.
 |
| Fuente: https://www.flickr.com/ |
En cuanto al temario de biología del año pasado, destacaría los siguientes contenidos: la bioquímica, el cuerpo humano (aparatos, sistemas...) y la biología celular.
En lo referente a los métodos de estudio que suelo emplear, me centro en la utilización de esquemas, mapas conceptuales, resúmenes, subrayado y, por supuesto, la memorización de los contenidos de la asignatura. Estos métodos siempre me han ayudado a obtener buenas calificaciones.
Dado que mi objetivo es estudiar medicina, necesito la calificación más alta. Por ello, me he propuesto esforzarme al máximo siendo constante y perseverante, estudiando diariamente y repasando los temas estudiados con anterioridad.
miércoles, 14 de septiembre de 2016
Louis Pasteur
Tras el experimento de Redi, gran parte de la sociedad seguía creyendo que la teoría de la generación espontánea era correcta. Por eso, el científico Louis Pasteur demostró que esta teoría era incorrecta a través del método científico.
 |
| Fuente: https://commons.wikimedia.org/wiki/File:Matraces-Pasteur.png |
Para confirmarlo, realizó una serie de experimentos. Primero, introdujo caldo en un recipiente cuyo cuello tenía forma de S y lo calentó. Con esto comprobó que los microbios se depositaban en el cuello del recipiente, pero si inclinaba el recipiente, el caldo comunicaba con el cuello y los microbios aparecían en dicho caldo.
Gracias a ello, demostró que el crecimiento de organismos en el caldo era debido a la contaminación por las bacterias del aire. Finalmente, analizó los resultados y llegó a la conclusión de que todos los seres vivos procedían de otros seres vivos, desechando así la teoría de la generación espontánea.
Suscribirse a:
Entradas (Atom)